Прежде всего, если речь идёт о резус-конфликте, необходимо диагностировать заболевание ещё в период внутриутробного развития плода, оценить его тяжесть и соответственно прогноз заболевания и проводить лечение до срока достижения плодом жизнеспособности. Все лечебно-профилактические методы, используемые в этот период жизни плода, подразделяют на неин- вазивные и инвазивные.
Неинвазивные методы
К неинвазивным методам относят плазмаферез и введение беременной внутривенного иммуноглобулина.
Плазмаферез беременной проводят с целью детоксикации, реокоррекции и иммунокоррекции.
Противопоказания к проведению плазмафереза:
Тяжёлое поражение сердечно-сосудистой системы;
Анемия (НЬ менее 100 г/л);
Гипопротеинемия (менее 55 г/л);
Гипокоагуляция;
Иммунодефицитное состояние;
Аллергические реакции в анамнезе на белковые и коллоидные препараты, антикоагулянты.
Иммуноглобулин для внутривенного введения применяют с целью ингибирования продукции собственных материнских антител и блокады Fc-связанных антител при их плацентарном транспорте. Используют иммуноглобулин для внутривенного введения в дозе 0,4 г на килограмм массы тела беременной. Эту дозу распределяют на 4-5 дней. Повторять курсы введения необходимо каждые 3 нед до родоразрешения. Данный метод лечения не считают общепризнанным, поскольку при тяжёлом течении заболевания исход для плода улучшается незначительно.
Инвазивные методы лечения
К инвазивным методам относят кордоцентез и внутриутробную трансфузию эритроцитарной массы. Данные процедуры осуществляют только при Rh-сенсибилизации, в настоящее время это единственный патогенетический метод лечения гемолитической болезни плода.
Показания для проведения кордоцентеза:
Отягощённый акушерский анамнез (гибель предыдущих детей от тяжёлых форм ГБПиН);
Высокий титр антител (1:32 и выше);
При УЗИ - признаки гемолитической болезни плода;
Высокие значения оптической плотности билирубина в околоплодных водах, полученных при амниоцентезе (3-я зона шкалы Лили).
Сроки, в течение которых проводят кордоцентез: с 24-й по 35-ю неделю беременности.
Показанием к проведению внутриутробной трансфузии эритроцитарной массы при обнаружении у плода положительного резус- фактора служит снижение показателей гемоглобина и гематокрита более чем на 15% от нормы, определяемой при данном сроке беременности. Для внутриутробной трансфузии эритроцитарной массы используют только «отмытые» эритроциты 0(1) группы крови Rh-отрицательные. Внутриутробную трансфузию эритроцитарной массы проводят по показаниям 1-3 раза.
Лечение гемолитической болезни новорождённого , в отличие от терапии гемолитической болезни плода, включает, в первую очередь, лечение гипербилирубинемии, во вторую - коррекцию анемии и, наконец, посиндромную терапию, направленную на восстановление функций различных органов и систем. Всех новорождённых с гемолитической болезнью не прикладывают к груди, а кормят искусственно в первые 5-7 дней жизни, поскольку антитела могут проникать с грудным молоком женщины и всасываться в кишечнике новорождённых, что приводит к усилению гемолиза.
Лечение гипербилирубинемии
Лечение гипербилирубинемии предполагает использование консервативной и оперативной терапии. Начинают с консервативного лечения, а при критических значениях билирубина сочетают с оперативным - заменным (обменным) переливанием крови (ЗПК).
Консервативная терапия включает фототерапию (ФТ) и применение иммуноглобулина для внутривенного введения. Инфузионную терапию, по рекомендации Российской ассоциации специалистов перинатальной медицины (РАСПМ), проводят в случаях невозможности адекватного выпаивания ребёнка. Фенобарбитал в настоящее время практически не используют в связи с тем, что начало эффекта значительно отсрочено от момента начала его применения и на фоне использования происходит усиление синдрома угнетения ЦНС.
Фототерапия
Механизм действия ФТ основан на том, что при её проведении на облучаемых участках в коже и подкожном жировом слое на глубине 2-3 мм в результате процессов фотоокисления и фотоизомеризации образуется водорастворимый изомер непрямого билирубина - люмирубин, который затем попадает в кровоток и выводится с жёлчью и мочой. Показания к ФТ:
Желтушность кожных покровов при рождении;
Высокая концентрация непрямого билирубина (табл. 8-1). Принципы проведения ФТ:
Доза облучения - не менее 8 мкВт/(см2хнм);
Следует соблюдать расстояние от источника до пациента, указанное в инструкции к аппарату;
Таблица 8-1. Минимальные значения концентрации непрямого билирубина (мкмоль/л), при которых показано проведение фототерапии
|
Масса тела, г |
Возраст |
|||
|
4-7 сут |
||||
Следует поместить ребёнка в кувез;
Следует защитить глаза и половые органы ребёнка;
Следует изменять положение ребёнка под лампами ФТ каждые. 6 ч.
ФТ проводят в постоянном режиме с перерывами на кормление ребёнка в течение 3-5 дней. Отменять ФТ следует при снижении содержания непрямого билирубина ниже 170 мкмоль/л.
При проведении ФТ могут возникнуть различные реакции и побочные эффекты, которые отражены в табл. 8-2. В ней же показаны и методы терапии, проводимой в таких случаях.
При появлении признаков холестаза, о чём свидетельствуют увеличение фракции прямого билирубина на 20-30% и более, повышение активности ACT и AJIT, щелочной фосфатазы, концентрации холестерина, время проведения ФТ следует ограничить до 6-12 ч/сут или совсем отменить во избежание развития синдрома «бронзового ребёнка».
Использование иммуноглобулина
Иммуноглобулин для внутривенного введения применяют с целью блокады Fc-рецепторов, что предотвращает гемолиз. Необходимо раннее начало введения иммуноглобулина (в первые 2 ч жизни), что возможно только при антенатальной диагностике гемолитической болезни. Более позднее введение иммуноглобулина возможно, но менее эффективно.
Используют стандартные иммуноглобулины для внутривенного введения: сандоглобин^, ISIVEN^ (Италия), полиглобин (Германия) и др.
Таблица 8-2. Осложнения и побочные эффекты фототерапии
|
Проявления |
Механизм развития |
Мероприятия |
|
Синдром «загорелой кожи» |
Индукция синтеза меланина |
Наблюдение |
|
Синдром «бронзового ребёнка» |
Накопление продуктов фотоокисления прямого билирубина |
Отменить ФТ |
|
Активация секреторной функции кишечника |
Наблюдение |
|
|
Лактазная недостаточность |
Серозные повреждения ворсинчатого эпителия |
|
|
Повреждение циркулирующих эритроцитов в результате фотосенсибилизации |
Отмена ФТ |
|
|
Ожоги кожи |
Чрезмерное излучение лампы |
Отмена ФТ |
|
Повышение потери жидкости |
Увеличить объём принимаемой ребёнком жидкости |
|
|
Кожные сыпи |
Повышение образования и выброса гистамина при фотосенсибилизации |
Наблюдение, при необходимости - отмена ФТ |
Возможные схемы введения иммуноглобулинов:
По 1 г/кг каждые 4 ч;
По 500 мг/кг каждые 2 ч;
По 800 мг/кг ежедневно в течение 3 дней.
Независимо от дозы и кратности получен доказанный (95%) положительный эффект, который проявлялся в существенном снижении частоты ЗПК и длительности фототерапии.
Иифузионная терапия
Инфузионную терапию проводят в тех случаях, когда нет возможности адекватно выпаивать ребёнка на фоне проводимой фототерапии. Суточный объём вводимой ребёнку жидкости необходимо увеличить на 10-20% (у детей с экстремально низкой массой тела - на 40%) по сравнению с физиологической потребностью.
При проведении инфузионной терапии следует следить за массой тела ребёнка, оценивать диурез, содержание электролитов, глюкозы крови, показатель гематокрита.
Инфузионная терапия включает преимущественно переливание 10% раствора глюкозы4. Инфузионную терапию проводят внутривенно или интрагастрально через желудочный зонд. Интрагастральное введение жидкости можно начинать с 3-4-го дня жизни, для профилактики развития холестаза в капельницу могут быть добавлены 25% раствор магния сульфата из расчёта 5 мл/кг, но-шпа* - 0,5 мл/кг, 4% раствор калия хлорида - 5 мл/кг. При интрагастральном введении жидкости нет необходимости уменьшать объём кормлений.
Оперативная терапия - заменное переливание крови
Различают раннее (в первые 2 сут жизни) и позднее (с 3 сут жизни) ЗПК.
Показанием для позднего ЗПК служат значения концентрации непрямого билирубина, равные 308-340 мкмоль/л (для доношенного новорождённого). Для недоношенного новорождённого критические цифры билирубина представлены в табл. 8-3.
Таблица 8-3. Показания для проведения позднего заменного переливания крови у новорождённых в зависимости от массы тела при рождении*
|
Масса тела, г |
Концентрация непрямого билирубина, мкмоль/л |
* Минимальные значения билирубина - показание к началу соответствующего лечения в случаях, когда на организм ребёнка действуют патологические факторы, повышающие риск билирубиновой энцефалопатии (гемолитическая анемия; оценка по шкале Апгар на 5-й минуте менее 4 баллов; Ра02 менее 40 мм рт.ст. длительностью более 1 ч; рН артериальной крови менее 7,15 длительностью более 1 ч; ректальная температура менее 35 °С; концентрация альбумина менее 25 г/л; ухудшение неврологического статуса на фоне гипербилирубинемии; генерализованное инфекционное заболевание или менингит).
При появлении первых симптомов билирубиновой интоксикации показано немедленное ЗПК независимо от концентрации билирубина.
Выбор препаратов для проведения заменного переливания крови
При изолированном Rh-конфликте используют резус-отрицательную одногруппную с кровью ребёнка эритроцитарную массу и плазму, но возможно использование плазмы AB(IV) группы крови. При изолированном групповом конфликте используют эритроцитарную массу 0(1) группы, совпадающую по резус-фактору с резус-фактором эритроцитов ребёнка, и плазму AB(IV) или одной группы с группой крови ребёнка. При возможности развития и Rh-несовместимости, и несовместимости по системе АВО, а также после внутриутробных гемотрансфузий для ЗПК используют резус-отрицательную эритроцитарную массу 0(1) группы крови и плазму AB(IV) или одной группы с группой крови ребёнка.
При гемолитической болезни новорождённого с конфликтом по редким факторам крови используют донорскую кровь, не имеющую «конфликтного» фактора.
Расчет объёма препаратов для заменного переливания крови
Общий объём составляет 1,5-2 ОЦК, т.е. для доношенного ребёнка около 150 мл/кг, а для недоношенного - около 180 мл/кг.
Соотношение эритроцитарной массы и плазмы зависит от исходной концентрации гемоглобина перед началом операции. Общий объём состоит из объёма эритроцитарной массы, необходимой для коррекции анемии, и объёма эритроцитарной массы и плазмы, необходимого для достижения объёма ЗПК. Объём эритроцитарной массы, необходимой для коррекции анемии, рассчитывают по формуле:
объём эритроцитарной массы (мл) = = (160 - НЬ ребёнка в г/л) х 0,4 х массу ребёнка в кг.
Из общего объёма следует вычесть объём эритроцитарной массы, необходимой для коррекции анемии; оставшийся объём восполняют эритроцитарной массой и плазмой в соотношении 2:1. Вышесказанному примерно соответствует следующее соотношение эритроцитарной массы в зависимости от концентрации
гемоглобина у ребёнка.
Эритроцитарная масса Плазма
120 г/л < НЬ <150 т/л = 2 1
100 г/л < НЬ <120 г/л = 3 1
80 г/л < НЬ <100 г/л = 4 1
Техника заменного переливания крови
ЗПК проводят через один из крупных сосудов (пупочную вену, подключичную вену). Перед ЗПК осуществляют забор крови для определения концентрации билирубина, совместимости крови донора и реципиента. ЗПК проводят «маятниковым способом», т.е. выводя и вводя поочерёдно порцию крови из расчёта до 5-7 мл на килограмм массы ребёнка. До начала ЗПК возможно введение плазмы из расчёта 5 мл/кг. Начинают ЗПК с выведения крови. До начала ЗПК и на его протяжении катетер промывают раствором гепарина натрия.
При исходной концентрации гемоглобина ниже 80 г/л ЗПК начинают с коррекции анемии, т.е. с введения только эри- троцитарной массы под контролем содержания гемоглобина. После достижения концентрации гемоглобина 160 г/л вводят эритроцитарную массу и плазму. Для этого можно развести эритроцитарную массу плазмой, а можно поочерёдно вводить два шприца эритроцитарной массы и один шприц плазмы.
По окончанию ЗПК повторно проводят забор крови для определения концентрации билирубина. После ЗПК продолжают консервативную терапию.
ЗПК может сопровождаться развитием немедленных и отсроченных побочных эффектов (табл. 8-4).
Поздняя анемия развивается через 2-3 нед после ЗПК. Обычно носит гипорегенераторный и гипоэритропоэтический характер. Для её коррекции используют рекомбинантный эритропоэтин (эпоэтин альфа подкожно 200 МЕ/кг один раз в три дня 4-6 нед).
При обнаружении дефицита железа на фоне лечения рекомби- нантным эритропоэтином в терапию включают препараты железа в дозе по утилизируемому железу 2 мг/кг внутрь.
Прогноз
При отёчной форме ГБПиН прогноз наименее благоприятный, что обусловлено тяжестью состояния ребёнка при рождении. При желтушной форме прогноз зависит от степени поражения ЦНС,
Таблица 8-4. Осложнения заменного переливания крови
|
Проявления |
Мероприятия |
|
|
Сердечные |
Контроль сердечной деятельности |
|
|
Объёмная перегрузка |
||
|
Остановка сердца |
||
|
Сосудистые |
Тромбоэмбол ия, воздушная эмболия |
Соблюдение техники переливания крови |
|
Промывание катетера раствором гепарина натрия |
||
|
Коагуляци- онные |
Передозировка гепарина натрия |
Контроль дозы гепарина натрия |
|
Тромбоцитопения |
Контроль количества тромбоцитов |
|
|
Электролитные |
Гиперкалиемия |
Для профилактики на каждые перелитые 100 мл (эритроцитарной массы и плазмы суммарно) ввести 1-2 мл 10% раствора кальция глю- коната |
|
Гипокальциемия |
||
|
Гипернатриемия |
Контроль |
|
|
Контроль КОС |
||
|
Инфекционные |
Вирусные |
Контроль доноров |
|
Бактериальные |
Для предупреждения осложнений после ЗПК и на время нахождения катетера в крупном сосуде назначают антибактериальную терапию |
|
|
Механическое разрушение донорских клеток |
Контроль |
|
|
Некротический энтероколит |
Наблюдение, обнаружение клинических симптомов, соответствующая терапия |
|
|
Гипотермия |
Контроль температуры тела, согревание |
|
|
Гипогликемия |
Для профилактики на каждые перелитые 100 мл (эритроцитарной массы и плазмы суммарно) ввести 2 мл 10% раствора глюкозы4 |
|
|
Реакция «трансплантат против хозяина» |
Переливать препараты крови, подвергшиеся облучению |
|
|
Не использовать большие объёмы для ЗПК |
||
выраженности билирубиновой энцефалопатии. При анемической форме прогноз наиболее благоприятный.
Перинатальная летальность при ГБПиН составляет 2,5%. Психическое и психомоторное развитие детей, перенёсших ГБПиН, у подавляющего большинства соответствует возрастным нормам. У 4,9% детей отмечают отставание в физическом развитии. Патологию ЦНС обнаруживают примерно у 8% детей.
Профилактика
Профилактика разработана для женщин, имеющих резус-отрицательную кровь. Профилактики групповой несовместимости не существует.
Для предупреждения развития резус-сенсибилизации всем женщинам, имеющим резус-отрицательную принадлежность крови, в первые 72 ч (желательно в первые сутки) после родов при резус-положительной крови у новорождённого или в случае аборта, как самопроизвольного, так и несамопроизвольного, следует ввести одну дозу анти-Э-резусного иммуноглобулина.
Гемолитическая болезнь новорожденных (ГБН) - заболевание, обусловленное несовместимостью крови матери и плода по различным антигенам, имеющимся в крови у последнего (наследуется от отца) и отсутствующим в крови матери. Чаще всего заболевание развивается при несовместимости крови матери и плода по резус-антигену (1 случай на 200-250 родов). Следует учесть, что имеется несколько типов резус-антигена, обозначаемых по Винеру - Rh 0 , Rh " , Rh " . По предложению Фишера-Рейса, типы резус-антигена стали обозначать соответственно буквами D, Е и С. Обычно резус-конфликт развивается при несовместимости по Rh 0 , т. е. (D)-антигену, по другим типам - реже. Причиной гемолитической болезни может быть и несовместимость по антигенам системы АВО.
Гемолитическая болезнь новорожденных возможна при несоответствии крови матери и плода и по другим антигенам: М, N, S, P или систем Лютеран (Lu), Леви (L), Келл (Кеll), Дюфи (Fy) и др.
Патогенез . При несоответствии крови матери и плода в организме беременной женщины вырабатываются антитела, которые затем проникают во время беременности через плацентарный барьер в кровь плода и вызывают разрушение (гемолиз) его эритроцитов. В результате усиленного гемолиза происходит нарушение билирубинового обмена. Нарушению последнего способствует недостаточность печени в виде незрелости ферментной системы глюкуронилтрансферазы. Последняя ответственна за конъюгацию непрямого билирубина с глюкуроновой кислотой и превращение его в нетоксичный прямой билирубин (билирубин-глюкуронид).
Возможны следующие варианты проникновения антител через плаценту:
- во время беременности, что приводит к врожденным формам ГБН (рождение мацерированных плодов, отечная, анемическая, желтушная формы);
- во время родов, что ведет к развитию послеродовой желтушной формы;
Антирезус-антитела образуются у 3-5 % женщин с резус-отрицательной кровью при беременности плодом с резус-положительной кровью. Обычно дети при резус-конфликте рождаются с ГБН от 2-3-й беременности, реже от 1-й беременности в случаях сенсибилизации в прошлом переливаниями крови без учета резус-фактора. У некоторых женщин количество антител может быть незначительно и антитела не проникают через плаценту, при этом у резус-сенсибилизированной женщины может родиться здоровый резус-положительный ребенок после рождения ею детей, страдавших ГБН. При АВО-несовместимости заболевание развивается уже при 1-й беременности.
Тяжесть ГБН неодинакова, зависит от количества антител, проникших от матери к плоду, компенсаторных возможностей организма плода. Гемолитическая болезнь новорожденных проявляется в 3 основных формах: анемической, желтушной, отечной.
Клиника . Гемолитическая болезнь новорожденных может проявиться в следующих вариантах:
- ребенок погибает в период внутриутробного развития (на 20-30-й неделе);
- рождается с универсальным отеком;
- в форме рано развившейся тяжелой желтухи или
- тяжелой анемии.
Общими симптомами для всех форм заболевания являются нормохромная анемия гиперрегенераторного характера с наличием в крови молодых форм эритроцитов (эритробластов, нормобластов, увеличенного количества ретикулоцитов), увеличение печени и селезенки.
Отечная форма болезни развивается при длительном действии изоантител во время беременности; плод не погибает, так как токсические продукты выводятся через плаценту в организм матери. Вследствие приспособительных реакций плода образуются очаги экстрамедуллярного кроветворения, увеличиваются селезенка (в 5-12 раз), печень, сердце, железы внутренней секреции. Нарушаются функции печени, особенно белковообразовательная, повышается проницаемость сосудов, развивается гипоальбуминемия. Все это ведет к выраженным отекам подкожного жирового слоя, накоплению жидкости в полостях (плевральной, брюшной) и увеличению массы плода почти в 2 раза против возрастной нормы. Резко выражены анемия (Нb 35-50 г/л, эритроцитов 1-1,5 x 10 12 /л), эритробластемия. Плацента резко увеличена, отечна. Обменные нарушения в некоторых случаях могут быть причиной смерти плода до рождения или во время родов. Отечная форма отличается крайне тяжелым течением и в большинстве случаев заканчивается летальным исходом. Ребенок, родившийся живым, умирает в течение ближайших минут или часов.
В настоящее время удается спасти некоторых детей с общим врожденным отеком путем осторожного применения заменных переливаний крови.
Желтушная форма развивается при воздействии изоантител на достаточно зрелый плод. Ребенок обычно рождается в срок, с нормальной массой тела, без видимых изменений цвета кожи. ГБН развивается через несколько часов поcле рождения. Уже в 1-2-е сутки его жизни выявляется желтуха, которая быстро усиливается; реже ребенок рождается с желтушной окраской кожи. Такую же окраску имеют околоплодные воды и первородная смазка. У всех детей с желтушной формой болезни отмечается увеличение печени, селезенки, лимфатических узлов, иногда сердца; повышение содержания билирубина в пуповинной крови - выше 51 мкмоль/л (у здоровых новорожденных он колеблется в пределах 10,2-51 мкмоль/л, составляя в среднем 28,05 мкмоль/л по Ван-ден-Бергу). В последующие 72 ч у детей с ГБН уровень билирубина интенсивно нарастает, почасовой прирост - от 0,85 до 3,4 мкмоль/л.
Определить почасовой прирост билирубина можно по формуле:
где В t - почасовой прирост билирубина; В n 1 - уровень билирубина при первом определении; В n 2 - уровень билирубина при втором определении; n 1 - возраст ребенка в часах при первом определении; n 2 - возраст ребенка в часах при втором определении билирубина.
Незрелость ферментных систем печени новорожденного приводит к накоплению в крови непрямого билирубина. Непрямой билирубин является цитоплазматическим ядом и приводит к повреждению гепатоцитов (клеток печени), мышечных клеток миокарда, но особенно нейронов (нервных клеток).
Интенсивное нарастание содержания непрямого билирубина (почасовой прирост от 0,85 до 3,4 мкмоль/л), если не принять меры по его снижению, довольно скоро (через 24-48 ч) приводит к его чрезмерному накоплению и появлению у ребенка резко выраженной желтухи с симптомами билирубиновой интоксикации и поражением центральной нервной системы (ядерная желтуха, или билирубиновая энцефалопатия), которая сопровождается ухудшением состояния ребенка: появляется вялость, ребенок хуже сосет, появляются частые срыгивания, рвота, нередко отмечаются тонические судороги (на 4-5-й день жизни), ригидность затылочных мышц, глазодвигательные нарушения и спазмы взора (симптом "заходящего солнца" - непроизвольный поворот глазных яблок книзу, в связи с чем между верхним краем роговицы и верхним веком видна полоска склеры); дыхание становится уреженным и нерегулярным, развиваются приступы цианоза, снижаются врожденные рефлексы Моро, Робинсона, Бабкина. Кроме того, происходит отложение кристаллического билирубина в мозговом слое почек - развивается билирубиновый инфаркт почек. Нарушение функции печени при ГБН проявляется не только нарушением образования прямого билирубина, но и снижением синтеза протромбина и белка. Уровень протромбина в крови снижается. Время кровотечения увеличивается. Нагрузка печени продуктами гемолиза часто приводит к нарушению фазы экскреции с развитием механической желтухи - так называемого синдрома сгущения желчи. При этом синдроме кал обесцвечен (обычно у детей с этой формой кал ярко-желтого цвета), печень еще более увеличивается, в крови повышается уровень прямого билирубина, в моче много желчных пигментов (реакция Гмелина положительная).
Токсические свойства непрямого билирубина начинают проявляться в том случае, когда он не связан с альбумином плазмы крови (снижена билирубинсвязывающая способность плазмы крови) и поэтому легко проникает за пределы сосудистого русла. При достаточном количестве альбумина в крови поражение мозга начинает развиваться при уровне билирубина, значительно превышающем критический.
Опасность поражения ЦНС в виде билирубиновой интоксикации (ядерной желтухи) появляется при повышении уровня непрямого билирубина у доношенного ребенка выше 306-340, у недоношенного - от 170 до 204 мкмоль/л. Возникающая билирубиновая энцефалопатия может привести к летальному исходу уже через 36 ч после рождения ребенка. Дети, остающиеся живыми, значительно отстают в психическом развитии.
В дальнейшем отмечается умеренная задержка общего развития ребенка. Вследствие угнетения механизмов иммунной защиты у таких детей легко развиваются пневмонии, омфалит, сепсис. Билирубиновая интоксикация, осложнения инфекционных заболеваний, анемия, изменения во внутренних органах обусловливают тяжелое течение врожденной желтушной формы ГБН с большим числом летальных исходов. Своевременное лечение больных позволяет предупредить неблагоприятные исходы этой формы ГБН.
Анемическая форма протекает, как правило, относительно легко. Она развивается в результате непродолжительного воздействия небольшой дозы изоантител матери на плод; при этом повреждения плода невелики, продукты гемолиза отводятся плацентой в организм матери. После рождения и прекращения функции плаценты при достаточной функции печени желтуха отсутствует, ребенок нормально развивается при наличии анемии. Эти случаи встречаются редко. Основным симптомом этой формы болезни является бледность кожных покровов в сочетании с низким количеством гемоглобина и эритроцитов, увеличением незрелых форм эритроцитов (эритробластов, нормобластов, ретикулоцитов). Печень и селезенка увеличены. Анемия развивается в конце 1-й - начале 2-й недели жизни, понижается содержание гемоглобина и эритроцитов, появляются анизоцитоз, полихромазия, эритробластоз. Печень и селезенка увеличены.
Обычно бледность кожных покровов отчетливо выявляется с первых дней жизни, но в более легких случаях она маскируется физиологической эритемой и транзиторной желтухой и отчетливо выявляется только к 7-10-му дню жизни. При дробных переливаниях резус-отрицательной крови быстро наступает выздоровление ребенка.
Развитие гемолитической болезни новорожденных не всегда определяется высотой титра изоиммунных антител у беременных. Имеет значение степень зрелости организма новорожденного - более тяжелое течение заболевания отмечают у недоношенных детей.
Гемолитическая болезнь новорожденных, связанная с несовместимостью крови матери и ребенка по антигенам системы АВО , встречается с той же частотой, что и ГБН, обусловленная резус-несовместимостью. ГБН, связанная с групповой несовместимостью, возникает в случаях, если мать имеет 0(I) группу крови, а ребенок А(II) или В(III). Обычно заболевание возникает при 1-й беременности. Клинически гемолитическая болезнь новорожденных, связанная с АВО-несовместимостью, протекает в легкой форме (в 90 % случаев), напоминая по течению транзиторную желтуху. Однако при частоте один случай на 2000-2200 родов заболевание может протекать в форме тяжелой желтухи и осложняться билирубиновой энцефалопатией, если своевременно не будут проведены активные мероприятия по снижению уровня билирубина, включая заменное переливание крови.
Причиной тяжелого течения процесса в таких случаях оказываются сопутствующие острые и хронические заболевания матери во время беременности, вызывающие повышение проницаемости плацентарного барьера для изоантител. ГБН, связанная с групповой несовместимостью, в форме отека не наблюдается.
Ранняя диагностика . Выделяют беременность, "угрожаемую" по развитию гемолитической болезни у плода. Предположение о возможности развития ГБН должно возникнуть при обследовании беременной в женской консультации. Резус-отрицательная кровь у матери и резус-положительная у отца, указания в анамнезе матери на переливание крови без учета резус-фактора должны вызывать предположение о возможности ГБН у будущего ребенка. Наличие отягощенного анамнеза (мертворождения, самопроизвольные выкидыши, рождение младенцев с ГБН, отставание в психическом развитии детей от предыдущих беременностей) заставляет думать о возможности тяжелого течения ГБН у ожидаемого ребенка и взятия такой женщины на особый учет с необходимостью проведения комплекса специальных исследований. В первую очередь должна быть обследована кровь женщины с резус-отрицательной принадлежностью на наличие резус-антител: при обнаружении последних должны быть проведены профилактические мероприятия, направленные на ослабление явлений изоиммунизации.
Диагноз заболевания у внутриутробного плода может быть установлен на основании результатов исследования околоплодных вод, полученных с помощью амниоцентеза (их оптической плотности, содержания в них билирубина).
Важным является установление диагноза ГБН с оценкой тяжести заболевания сразу после рождения ребенка. Критериями наличия заболевания являются: резус-отрицательная кровь матери и резус-положительная кровь у новорожденного с наличием в крови у матери резус-антител; при групповой несовместимости - наличие 0(I) группы у матери и А(II) или В(III) - у ребенка с определением в сыворотке крови матери высокого титра изоиммунных α- или β-агглютининов в белковой среде.
Таблица 1. Дифференциально-диагностические симптомы при Rh- и AВ0-несовместимости
| Несовместимость | Проявления | ||||||||
| Клинические | Параклинические | ||||||||
| Общее состояние | Желтуха | Aнемия | Печень, селезенка | Реакция Кумбса | Реакция Мунка Андерсена | Эритробласты, рeтикулoциты | Морфология эритроцитов | ||
| появление | интенсивность | ||||||||
| Rh | нарушенное | до 14 ч | + + + | + - + + | увеличены | + | (-) | + + | макроциты |
| АВ0 | хорошее | 1-2 дня | + - + + | - | не увеличены | (-) | (+) | + | сфероциты |
Как правило, в случае крайне тяжелого течения ГБН диагноз не вызывает затруднений даже при отсутствии анамнестических данных; околоплодные воды и родовая смазка окрашены в желтый или зеленый цвет, ребенок отечный, желтушный или бледный, значительно увеличены печень и селезенка.
В случаях, когда состояние неясно, для раннего диагноза и прогноза заболевания имеет значение клинический анализ крови новорожденного, особенно пуповинной, так как изменения в ней при ГБН выявляются значительно раньше, чем другие клинические признаки заболевания.
На наличие ГБН указывают следующие показатели пуповинной крови:
- гемоглобин ниже 166 г/л;
- наличие эритробластов и нормобластов в количестве более 10 на 100 лейкоцитов;
- положительная проба Кумбса при резус-конфликте; при конфликте по системе АВО проба Кумбса отрицательная;
- содержание билирубина выше 51 мкмоль/л по Ван-ден-Бергу;
- снижение уровня белка крови до 40-50 г/л.
Если пуповинная кровь для исследования не была взята, то при возникновении подозрения на наличие гемолитической болезни в связи с ранним появлением желтухи (в первые сутки после рождения) необходимо оценить тяжесть гемолитической болезни по данным почасового прироста билирубина.
Трудно бывает рано установить диагноз в случаях, когда ГБН вызвана другими антигенами. Для этого проводится исследование сыворотки крови матери на наличие антител к редким антигенам. Пока выясняется причина, вызвавшая заболевание, лечение должно быть направлено на борьбу с интоксикацией непрямым билирубином.
Дифференциальный диагноз . В диференциально-диагностическом отношении следует в основном иметь в виду гипербилирубинемии с повышением непрямого билирубина и гипербилирубинемии, при которых существует гемолиз, т. е. которые протекают с эритробластозом и ретикулезом в периферической крови:
- вследствие врожденных или приобретенных дефектов мембраны эритроцитов с типичными изменениями их морфологии, как сфероцитоз, элиптоцитоз, стоматоцитоз и пикноцитоз;
- в результате энзиматических дефектов эритроцитов - глюкозо-6-фосфатдегидрогеназы (наиболее частое энзиматично-метаболическое заболевание), пируваткиназы и пр.
Основными дифференциально-диагностическими критериями являются положительные тесты Кумбса или Мунка-Андерсена при гемолитической болезни новорожденного и доказывание энзиматической недостаточности. Сюда относятся и талассемии, и диссеминированная внутрисосудистая коагулопатия. Для подтверждения диагноза альфа-талассемии значение имеет фамильный анамнез ребенка и, в основном, установление посредством гемоглобинового электрофореза гемоглобина Барта. Установлению диагноза при диссеминированной внутрисосудистой коагулопатии способствуют характерные изменения факторов свертывания крови или глобальные тесты, как протромбиновое время, тромбиновое, гепариновое время, число тромбоцитов, фрагментированные эритроциты.
Менее известными и более трудно диагностируемыми являются метаболические эндокринные гипербилирубинемии. Синдром Криглера-Найяра (семейная негемолитическая гипербилирубинемия с ядерной желтухой) характеризуется гипербилирубинемией непрямого типа без данных на гемолиз и передается как аутосомно-рецессивное заболевание. У родителей наблюдается пониженная способность к конъюгации билирубина без желтухи. Желтуха у ребенка проявляется уже в первые дни после рождения, иногда с весьма высокими величинами билирубина. В связи с этим может возникнуть необходимость и в обменном переливании крови.
Транзиторная семейная неонатальная гипербилирубинемия или синдром Люцейя-Дрисколла проявляется в повышении непрямого билирубина без данных, указывающих на гемолиз. Считают, что она возникает под влиянием ингибирующего воздействия какого-то фактора, по всей вероятности, стероида у беременных, нарушающего нормальную конъюгацию билирубина. При резко выраженной желтухе у некоторых детей необходимо обменное переливание крови.
Желтуха регулярно сопутствует гипотиреоидизму новорожденных с их характерным видом, гипотонией, грубым голосом, большим животом и в основном с отставанием в развитии костных ядер и специфическими отклонениями уровня тиреоидных гормонов. У детей наблюдается гипербилирубинемия непрямого типа, встречаемая у новорожденных с гипопитуитаризмом или анэнцефалией. Резко выраженную желтуху при этих двух группах заболеваний связывают с наличием гипотиреоидизма.
Многие лекарственные средства, гормоны и другие вещества и состояния играют роль в появлении гипербилирубинемии у новорожденных детей, как, например, сульфаниламиды, витамин К, в особенности в больших дозах, новобиоцин, гипоксия, ацидоз и пр. Три α-20-β-прегнадиол и молоко некоторых матерей также являются причиной этого болезненного состояния.
У новорожденных, матери которых больны сахарным диабетом, гипербилирубинемия с повышением непрямого билирубина без гемолиза наблюдается чаще и выражена сильнее, чем у здоровых новорожденных. Она появляется к 3-му дню после рождения, когда повышается и гематокрит, чем в настоящее время объясняется гипербилирубинемия у этих детей.
Желтуха и анемия может наблюдаться при сепсисе, цитомегалии, токсоплазмозе, врожденном инфекционном гепатите, сифилисе и других заболеваниях.
Лечение ГБН - комплексное, направленное на быстрейшее удаление из организма новорожденного токсических продуктов гемолиза, главным образом непрямого билирубина, а также антител, способствующих продолжению гемолитического процесса, и на повышение функциональной способности различных систем и органов, особенно печени и почек.
Наиболее эффективным методом борьбы с гипербилирубинемией при тяжелых и средней тяжести формах заболевания является раннее обменное переливание крови из расчета 150-180 мл/кг массы новорожденного. При резус-конфликте переливают одно-группную резус-отрицательную кровь, при АВО-конфликте - эритроциты 0(I) группы, суспендированные в плазме АВ(IV) группы. Для обменного переливания кровь донора (стабилизаторы 7, 5) должна быть свежей, не более 3 сут хранения после забора.
Показанием к обменному переливанию крови является:
- увеличение содержания билирубина в плазме крови в первые сутки до 171,04 мкмоль/л
- нарастание билирубина в крови на 0,85 мкмоль/л в час
Рано примененное обменное переливание крови позволяет корригировать анемию, вывести значительную часть сенсибилизированных эритроцитов, что, в свою очередь, ограничивает развитие гемолитического процесса и устраняет некоторое количество билирубина до его распределения в более значительных количествах в экстраваскулярном пространстве. При наличии тяжелой анемии (гематокрит 35% или меньше) применяют обменное переливание крови - 25-80 мг/кг массы тела эритроцитной массы через 30 мин после рождения с целью увеличить гематокрит до 40%. Указывается на возможность появления гиповолемии у таких детей. Поэтому рекомендуется перед тем, как приступить к манипуляциям с целью изменения объема крови, провести тщательное измерение венозного и артериального давления.
Наиболее целесообразно и технически легко выполнимо проведение обменного переливания через пупочную вену (первые 3-5 дней жизни). Через катетер, введенный в пупочную вену, сначала выпускают 10 мл крови, затем вводят такое же количество крови донора, продолжительность процедуры - 1 ½ — 2 ч (скорость операции по замене крови - 2-3 мл/мин), в конце трансфузии вводят на 50 мл крови больше, чем выводят. После замены каждых 100 мл крови ребенку необходимо ввести внутривенно 1 мл 10 % раствора кальция хлорида. После переливания крови проводится дезинтоксикационная терапия: обильное введение жидкости внутрь, внутривенное переливание плазмы, альбумина, глюкозы (100-250 мл).
В связи с тем, что лимонная кислота консервированной крови для обменного переливания весьма быстро метаболизируется в печени до бикарбонатов, у большей части детей не наблюдается никаких затруднений во время самой трансфузии без ощелачивания, если ее производить очень медленно. Однако после трансфузии у некоторых новорожденных развивается алкалоз, который может продолжаться в течение 72 ч. Опасно производить вливание крови, консервированной с помощью кислоты, так как это может повлиять непосредственно на миокард и вызвать остановку сердечной деятельности. В связи с этим у детей, находящихся в состоянии шока или значительного метаболического ацидоза, рекомендуется применять алкализированную кровь. С другой стороны, не следует забывать, что с введением алкализирующих средств существует опасность повышения осмолярности с его последствиями. Устранение 60 мл плазмы из крови донора перед обменным переливанием крови уменьшает кислотность и нагрузку цитратами и нормализует гематокрит.
Некоторые авторы рекомендуют использовать при обменном переливании гепаринизированную кровь. Следует отметить, что содержание ионизированного кальция, электролитов, кислотно-щелочной баланс и уровень сахара крови не изменяются. Но как последствие при применении гепарина значительно повышается уровень неэстерифицированных жирных кислот, которые могут заменить билирубин в комплексе альбумин-билирубин. Следует иметь в виду также и возможные изменения коагуляционных параметров у новорожденного. Наиболее важным недостатком гепаринизированной крови при ее использовании для обменного переливания является то, что ее следует применить не позже 24-ого часа от момента взятия ее от донора и консервирования.
Из изложенного следует, что обменное переливание крови у новорожденных сопряжено с рядом осложнений, если не учитывать биохимические изменения, которые могут наступить во время этой манипуляции.
Для улучшения функции печени применяют фенобарбитал. Лечение фенобарбиталом обусловлено его индуцирующим действием на активность глюкоронилтрансферазы и установленной повышенной способностью лигандина связывать билирубин в гепатоците. Его применяют уже с первого-второго дня в дозе 5 мг/кг массы тела 2-3 раза в сутки, некоторыми клиницистами рекомендуется до 10 мг/кг массы тела в сутки. Считают, что это лечение не может дать результата при уже проявленной желтухе.
При нарушении билирубинвыделительной функции печени и развитии "синдрома сгущения желчи" можно назначить внутрь 5-10% раствор магния сульфата по 5 мл 2-3 раза в день, 10-20% раствор ксилита, холосас, сорбит. Эффективным также является дуоденальное зондирование с целью желчного дренажа. Однако лечение с помощью агара, активированного угля и сернокислой магнезии с целью редукции энтерогепатальной циркуляции и резорбции билирубина отвергается большинством авторов на основе повседневной практики, поскольку не дает положительных результатов.
Ребенку назначают: кормление донорским молоком, прикладывание к груди не ранее 10-12-го (по показаниям и позже) дня жизни, аденозитрофосфорную кислоту (АТФ) по 0,5 мл внутримышечно, метионин, аскорбиновую кислоту, пиридоксин, цианокобаламин, токоферол по 10 мг через рот. Внутрь назначают также преднизолон по 1-1,5 мг/кг в течение 7-8 дней.
Показана также фототерапия (облучение новорожденных лампами "синего или голубого" света): сеансы по 3 ч с интервалами 1-2 ч, т.е. до 12-16 ч в сутки (фототерапия занимает от 2 до 6 сут). Под действием света билирубин окисляется, превращаясь в биливердин и другие нетоксические вещества.
В настоящее время фототерапия является наиболее подходящим методом регулирования уровня билирубина у новорожденных. Данные статистики показывают, что после внедрения фототерапии в практику число обменных переливаний крови уменьшилось значительно. В основе метода лежит фотоизомеризация билирубина-IХ-α и получение фотобилирубина, весьма быстро выделяющегося с желчью. Этот процесс осуществляется в коже и ее капиллярной сети на глубине 2 мм. Показаниями к проведению этого лечения являются в основном гипербилирубинемия недоношенных при Rh- и АВО-несовместимости, обычно после обменного переливания крови. Имеются сообщения о более благоприятном эффекте фототерапии, чем обменном переливании крови у новорожденного с негемолитической гипербилирубинемией. Индикации для включения фототерапии указаны на табл. 2, в которой каждый отдельный случай оценивается в зависимости от постнатального возраста, массы тела при рождении, патологии при рождении и уровня билирубина.
При наличии перинатальной гипоксии, респираторного дистресса, метаболического ацидоза (рН 7,25 или ниже), гипотермии (ниже 35°), низкого сывороточного белка (50 г/л и ниже), церебральных нарушений, массы тела при рождении меньше 1500 г и симптомов клинического ухудшения следует применить фототерапию и обменное переливание крови, как при последующей, более высокой билирубиновой группе, указанной в табл.2.
Таблица 2. Основные направления при лечении гипербилирубинемий (по Brown и сотр.)
| Сывороточный билирубин (мкмоль/л) |
Масса тела при рождении |
< 24 ч | 24-48 ч | 49-72 ч | > 72 |
| 85,52 | Все | Под наблюдением | |||
| 85,52 - 153,93 | Все | Фототерапия при гемолизе | Под наблюдением | ||
| 171,04 - 239,45 | < 2500 г | Обменное переливание крови при гемолизе | Фототерапия | ||
| > 2500 г | Исследование при уровне билирубина 12 мг | ||||
| 256,56 - 324,9 | < 2500 г | Обменное переливание крови | Иногда обменное переливание крови | ||
| > 2500 г | Фототерапия | ||||
| 342,08 | Все | Обменное переливание крови | |||
Однако при более продолжительном применении фототерапия ведет к ряду побочных явлений: поражение сетчатки, отклонения эмбриогенеза (опыты на животных), тробмоцитопения, бледность кожных покровов и синдром "медного ребенка", наблюдающийся при данных, указывающих на холостаз. Предполагается, что задержка какого-то продукта, полученного при фототерапии, является причиной этого специфического цвета кожи у ребенка. Как побочные явления описывают также и наличие зеленых фекалий и потерю жидкостей и некоторых солей с фекалиями.
В практике необходимо иметь в виду следующие предохранительные меры:
- Перед применением фототерапии следует, по возможности, определить этиологию гипербилирубинемий во избежание пропуска угрожающего жизни состояния
- Осуществлять защиту глаз и гонад
- Контролировать температуру ребенка
- Контролировать водный баланс (2 раза в день измерять у ребенка температуру, количество и удельную массу мочи, гематокрит) и при необходимости вводить большее количество жидкости
- Исследовать билирубин каждые 12 ч, а при показаниях и чаще, не рассчитывая на оценку тяжести желтухи по цвету кожи
- Контролировать число тромбоцитов
- Исследовать гематокрит, в особенности при гемолитической болезни
- Применять питательную смесь без лактозы при диспептических фекалиях, содержащих увеличенное количество редуцирующих веществ
Вопрос о повторных заменных переливаниях крови решается по темпам нарастания уровня билирубина в динамике. У доношенных новорожденных такие показания возникают при почасовом приросте содержания билирубина более 5,13 мкмоль/л, или следует ориентироваться на уровень билирубина, который превышает критические цифры (по шкале Полачека): уровень непрямого билирубина у доношенных свыше 306 и у недоношенных - свыше 204 мкмоль/л.
При развитии у ребенка анемии (снижение гемоглобина ниже 80 г/л) проводят антианемическое лечение путем дробных переливаний крови по 20-25 мл 2-3 раза. Дети с ГБН нуждаются во внимательном уходе, правильном вскармливании.
Если ребенок не получал заменного переливания крови, то его необходимо в течение первых 2-3 нед кормить донорским молоком, ориентируясь при этом не только на содержание резус-антител в молоке матери, но и на тяжесть течения болезни.
Детей, леченных заменными переливаниями крови, кормить молоком матери можно начинать в более ранние сроки (с 5-7-го дня жизни).
После проведенного лечения в остром периоде заболевания, при выписке из родильного дома или больницы ребенку необходимо с 3-недельного возраста до 2 мес каждые 10-14 дней делать анализ крови и при снижении гемоглобина провести курс лечения витамином В 12 по 50 мкг через день, 10-12 инъекций на курс. Детям с поражением центральной нервной системы назначают курс витамина В 12 - по 50 мкг через день, на курс 20 инъекций.
Прогноз . Дети, перенесшие гемолитическую болезнь новорожденных и своевременно леченные достаточными по объему обменными переливаниями крови, в дальнейшем обычно хорошо развиваются. При легкой и средне-тяжелой формах желтухи прогноз благоприятный. Больные ГБН в форме тяжелой желтухи с гипербилирубинемией выше "критических" цифр в остром периоде, не леченные своевременно заменными переливаниями крови, могут погибнуть в течение первых дней жизни. У оставшихся в живых при развитии в остром периоде ядерной желтухи в дальнейшем обнаруживается органическое поражение ЦНС, которое проявляется отставанием в физическом и психическом развитии, поражением слуха и нарушением речи.
Дети с остаточными явлениями в состоянии ЦНС нуждаются в восстановительной терапии. За ними должен быть налажен хороший уход, им проводится массаж, назначается медикаментозная терапия - глутаминовая кислота, витамины комплекса В (В 6 , В 1 , В 12), аминалон.
Профилактические мероприятия для предупреждения ГБН или уменьшения ее тяжести должны проводиться уже в женской консультации и заключаются в следующем:
- Определение резус-фактора и группы крови у всех беременных женщин
- Всех женщин с резус-отрицательной кровью и с 0(I) группой необходимо брать на учет, собирать у них подробный анамнез, выяснять, не делали ли им в прошлом переливание крови без учета резус-фактора. У всех этих женщин регулярно (1 раз в месяц) необходимо определять титр резус-антител. При неблагоприятном (по ГБН) анамнезе, высоком титре антител проводят досрочное (за 2 нед) родоразрешение.
- В настоящее время успешно проводят десенсибилизацию с резус-отрицательной кровью путем ряда специальных мероприятий: в последние 3 мес беременности - это подсадка кожного лоскута от мужа, введение первобеременной (если у ребенка резус-положительная кровь) сразу после родов (в течение первых 72 ч после рожддения) антирезус-гамма- иммуноглобулина (200-250 мкг), приготовленного из крови резус-отрицательных женщин, родивших резус-положительного ребенка. Этим путем ставится цель обезвредить Rh-фактор как антиген.
- Беременных с резус-отрицательной кровью, у которых быстро нарастает титр антител, особенно если предыдущие беременности заканчивались неблагополучно, за 3-4 нед до родов следует помещать в специализированный родильный дом для контроля за течением беременности. У беременных с высоким титром антител, находящихся в стационаре, необходимо следить в динамике за уровнем билирубина у плода. При высоких титрах билирубина может оказаться необходимым более раннее родоразрешение, если будет констатирована оптимальная степень зрелости плода (что возможно при современных исследованиях), позволяющая ему справиться с внеутробной жизнью. Описаны случаи проведения внутриутробного обменного переливания крови у плода.
- При резус-отрицательной крови необходимо сохранять первую беременность, так как обычно первый ребенок рождается нормальным, угроза ГБН у детей таких женщин возрастает при повторных беременностях.
Низкий гемоглобин у новорожденных грозит тяжелыми осложнениями. С таким состоянием, как гемолитическая болезнь новорожденных, сталкивается врач примерно в 0,6% родоразрешений. При этом характерен низкий гемоглобин у недоношенного ребенка, нежели у рожденного в срок. Справиться с состоянием поможет такая манипуляция, как заменное переливание крови у новорожденных.
Об анемии у младенцев говорят, когда гемоглобин на 1-2 неделе жизни не превышает 140 г/л, а эритроциты 4,5*10 12 /л, гематокрит при этом снижается менее 40%. С 3-4 недели внеутробного развития нижней границей нормы является 120 г/л и эритроциты 4,0*10 12 /л.
Причины развития анемии у новорожденного объединяют в три группы:
- Постгеморрагические – в результате кровопотери при разрыве пуповины, патологии плаценты, кровоизлияний в полости тела, кефалогематомы, кровотечений из кишечника и прочее.
- Гемолитические – причина в патологическом разрушении эритроцитов при иммунных процессах, токсическом воздействии, радиации. Примером служит гемолитическая болезнь плода и новорожденного при резус-конфликте.
- Апластические, гипопластические или дефицитные – недостаточность синтеза эритроцитов. Пример – ранняя анемия у недоношенных.
- Смешанная форма – примером является снижение гемоглобина при генерализованных инфекциях. Включает железодефицитную, гемолитическую, гипопластическую и другие формы.
Ранняя анемия недоношенных детей, РАН, развивается в 1-2 месяц неонатального периода. Основной причиной этого состояния является соответствие больших темпов роста массы тела и ОЦК со способностью эритропоэза воспроизводить новые эритроциты. У недоношенных продукция эритропоэтина значительно уступает таковой у зрелых младенцев.
Анемия у недоношенных детей с массой тела до 1500 кг зачастую связана с флеботомическими потерями – в результате забора крови на анализы. Переливание эритроцитарной массы при низком гемоглобине у таких малышей в 15% случаев спровоцировано именно забором крови.
Гемолитическая болезнь новорожденных
Причины
Гемолитическая болезнь новорожденных, или ГБН – это состояние, связанное с развитием иммунологического конфликта крови матери и плода, когда антигены размещаются на эритроцитах ребенка, а антитела к ним вырабатывает материнский организм.

Заметить гемолитическую болезнь плода и предотвратить ее дальнейшее развитие можно уже на 18-24 неделе гестации. В первую неделю жизни обнаруживается анемия новорожденных, в некоторых случаях уровень гемоглобина у грудного ребенка может снижаться на первых месяцах жизни как результат гемолиза эритроцитов внутриутробно.
Основой развития иммунологического конфликта является сенсибилизация антигеном положительного резус фактора, когда он попадает в кровоток мамы. Это произойти может в результате прошлых беременностей, особенно которые закончились абортом или травматичными родами, гестозом, экстрагенитальной патологии у матери.
Во время гестации в норме эритроциты плода поступают в организм мамы в мизерных количествах – 0,1-0,2 мл, а в период родов – 3-4 мл. Но уже этого хватит, чтобы произошел первичный иммунный ответ и выработались антитела. Они относятся к иммуноглобулинам класса М, которые весьма громоздки, чтобы проникнуть через плаценту. Поэтому ребенку от первой беременности с большой вероятностью не грозит гемолитическая болезнь новорожденных.
В период повторных гестаций вырабатывается иммуноглобулин класса G, который с легкостью проникает в кровоток плода и вызывает гемолиз его эритроцитов, уровня гемоглобина плода стремительно падает, а билирубин растет.
Классификация
Существует несколько вариантов внутриутробной несовместимости мамы и ребенка:
- по резус-фактору, когда мама Rh-, а плод Rh+;
- по группе, если мать 0 (Ⅰ), у плода — А (Ⅱ), В (Ⅲ) группы;
- редкие варианты, когда возникает конфликт по системам Kell, Duffi, Kidd и др.
По клиническим симптомам ГБН классифицируют таким образом:
- отечная форма;
- желтушная;
- анемичная.
Гемолитическая болезнь плода ГБП

Желтушная форма прогрессирует незадолго до родов, гемолиз столь выражен, что в крови накапливается огромное количество непрямого билирубина. Он депонируется в ядрах головного мозга, вызывая церебральные проявления вплоть до комы.
Анемичная форма является самой безопасной, развивается в ответ на внедрение небольшого количества антигена в кровоток матери перед родами. Кроме снижения гемоглобина, младенцы не имеют осложнений.
Симптомы ГБН
При рождении с ГБН имеются симптомы согласно форме заболевания. Отечная форма характеризуется такими симптомами:
- массивные отеки от пастозности до анасарки;
- развитие у младенцев желтухи и низкого гемоглобина;
- печень и селезенка при этом увеличены;
- выраженные геморрагические проявления: нарушение свертываемости крови;
- недостаточность сердечно-легочная;
- желтуха незначительная.
Желтушная форма:
- желтуха;
- гепатоспленомегалия;
- застой желчи;
- при повышении уровня билирубина возникают неврологические симптомы;
- развитие билирубиновой энцефалопатии – 1 стадия обратимая с вялостью, нарушением сосания, апноэ, 2 стадия – опистотонус, ригидность затылочных мышц, судороги, 3 и 4 стадии с прогрессирующим ухудшением.
Анемичная форма:
- бледность кожи и слизистых;
- гемоглобин понижен у грудничка вплоть до 2 месяцев;
- вялость и адинамичность;
- тахикардия;
- гепатоспленомегалия.
Тяжелее протекает заболевание у недоношенных детей.
Заменное (обменное) переливание крови у новорожденных
Показания

Гемолитическая болезнь новорожденных может привести к тяжелым осложнениям и даже смерти ребенка. Устранить это жизнеугрожающее состояние способна заменная, или обменная, гемотрансфузия новорожденному взамен собственной, подвергнувшейся гемолизу крови.
Показаниями для операции заменного переливания крови ЗПК по Даймонду являются:
- лечение отечной формы ГБН;
- безрезультатная фототерапия при желтушной.
Выделяют раннее ЗПК и позднее. Первое осуществляется в 2 дня от рождения, а второе – с третьих суток.
Лабораторными данными, указывающими на необходимость раннего заменного переливания, являются для доношенный новорожденных:
- билирубин из пуповины – 68 мкмоль/л;
- почасовой прирост билирубина более 9 мкмоль/л.
Требования к началу заменного переливания крови при низком гемоглобине у недоношенных детей жестче – почасовой прирост билирубина должен быть не более 8 мкмоль/л . Это связано с несостоятельностью ферментативной системы недоношенного.
Позднее заменное переливание крови (с третьих суток) показано у доношенных детей, когда билирубин более или равен 342 мкмоль/л. У недоношенных же малышей прибегают к позднему ЗПК в зависимости от массы тела при рождении и возраста. Ниже представлена таблица этой зависимости.
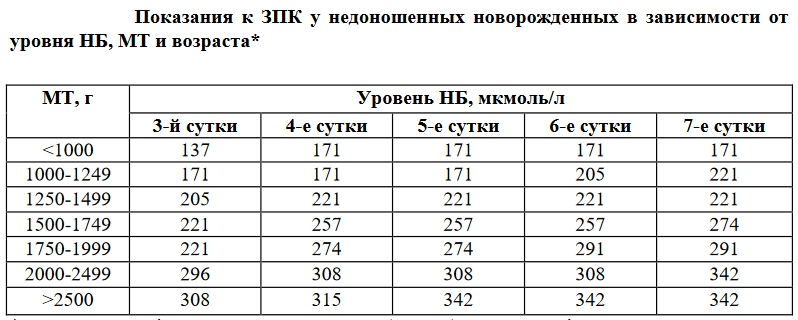
Важно знать, что операция заменного переливания крови может проводиться и раньше, когда непрямой билирубин не достиг своих критических значений. Это возможно, если имеются предикторы билирубиновой энцефалопатии:
- на 5-ой минуте после рождения по Апгар ребенок оценен менее чем в 3 балла;
- общий белок ниже 50 г/л, а альбумин – 25 г/л;
- глюкоза < 2,2 ммоль/л;
- факт генерализации инфекции или менингита;
- парциальное давление углекислоты на выдохе до 40 мм.рт.ст длительностью более 1 часа;
- рН артериальной крови менее 7,15 более 1 часа;
- ректальная температура равна или менее 35 градусов;
- усугубление неврологической симптоматики при гипербилирубинемии.
Что переливают
Если имеется тяжелая гемолитическая болезнь новорожденного, то незамедлительно используют методику частичной операции ЗПК, когда вводят эритроциты первой группы отрицательного резус фактора до определения группы и резуса в ребенка. Доза – 45 мл/кг.
Если у младенца имеется несовместимость только по резус-фактору, то ему переливают резус-отрицательную эритроцитарную массу или отмытые эритроциты его же группы и свежезамороженную плазму, можно и Ⅳ группы. Нельзя применять резус-положительные эритроциты.
При операции ЗПК использовать только свежеприготовленные эритроциты – не позднее 72 часов от забора.
Если конфликт по группе крови, то используют эритроцитарную массу или отмытые эритроциты первой 0(Ⅰ) группы, с резусом как у эритроцитов ребенка, плазма АВ (Ⅳ) или группы крови ребенка. Нельзя переливать эритроциты той группы, что и младенца.
Если есть комбинация несовместимости по группе и Rh-фактору, а также когда внутриутробно проводила ЗПК, то вливают эритроцитарную массу 0 (Ⅰ) группы Rh-отрицательную и плазму АВ (Ⅳ) или той же группы, что и ребенок.
Если имеется несовместимость по редким факторам, то применяют для переливания донорские эритроциты, не имеющие антигена.

Как подбирать дозу
Общий объем среды для введения должен составить 2 объема циркулирующей крови новорожденного, а это 160-180 мл/кг – доношенные, 180 мл/кг – недоношенные дети. Отношение эр.массы к плазме в этом объеме будет определяться исходным уровнем гемоглобина. Общие объем ОЗПК включает в себя эритроциты, необходимые для коррекции анемии у новорожденного+эритроцитарную массу и плазму, требуемую для достижения объема ЗПК.
Эр. масса в мл = (160 — НЬ (г/л) фактический) х 0,4 х массу ребенка (кг).
Полученную цифру нужно отнять от общего объема для ЗПК. После этого оставшийся объем восполняется эритроцитарной массой и плазмой в соотношении 2:1.
Подготовка к ЗПК
Перед тем как проводить операцию по обменному переливанию крови, необходимо выполнить такие условия:
- устранить ацидоз, гипоксемию, гипогликемию, гипотонию, гипотермию;
- подготовить кювез с источником лучистого света;
- исключить энтеральное питание за 3 часа до процедуры;
- постановка желудочного зонда для периодического удаления содержимого;
- выполнить очистительную клизму;
- подготовка инструментов: пупочные катетеры, шприцы различного объема и прочее;
- согревание трансфузионной среды;
- организовать все необходимое для реанимационных мероприятий;
- кровь донора должна быть проверена на групповую принадлежность и совместимость с сывороткой реципиента;
- перед выполнением процедуры соблюдать асептику, обкладывать область манипуляции стерильными салфетками, провести обработку рук врача и области операции.
Методика

После подготовительного этапа врач и ассистент выполняют такие манипуляции заменного (обменного) переливания крови.
- После отсечения верхушки пуповинного остатка вводят стерильный катетер на 3-5 см (у крупных детей 6-8 см) по направлению к печени. При позднем переливании крови после 4 дней от рождения или с имеющимися противопоказаниями постановки пупочного катетера переливание выполняют через другую доступную центральную вену.
- Катетер заполняется гепаринизированным раствором 0,5-1 ЕД/мл.
- Выводят (забирают) кровь ребенка по 10-20 мл, а у недоношенных по 5-10 мл.
- Вводят эритроцитарную массу и плазму в эквиваленте забранной. После 2 шприцев эр.массы следует 1 шприц плазмы.
- После замещения 100 мл объема необходимой инфузии нужно ввести 1-2 мл раствора кальция глюконата или 0,5 мл раствора кальция хлорида в 5-10 мл раствора глюкозы 10%.
- Завершить операцию после замещения 2 объемов циркулирующей крови. Продолжительность процедуры должна составлять 1,5-2,5 часа.
- Перед завершением нужно забрать кровь для оценки билирубина.
- Перед удалением катетера ввести половину суточной дозы антибиотика.
- После завершения процедуры на ранку наложить стерильную повязку.
Об эффективности проводимой операции заменного переливания говорит более чем двукратное падение концентрации билирубина уже к концу манипуляции.
В послеоперационном периоде необходим обязательный контроль за гликемии, кальцием, калием, значением кислотности, гемодинамикой, инфекционным заражением. Дальнейшее лечение включает фототерапию. Если формируется поздняя анемия – назначают препараты эритропоэтина – Эпоэтин альфа.
Осложнения
Самыми тяжелые осложнения развиваются сразу после ОЗПК:
- аритмия;
- прекращение работы сердца;
- тромбозы;
- гиперкалиемия;
- тромбоцитопения;
- возникновение инфекции;
- гипокальциемия;
- ацидоз;
- гипотермия;
- некротический энтероколит.
- Гилербилирубинемия, всегда выясните причину!
- Анемия при водянке плода (эритробластоз).
- Полицитемия (гематокрит > 70 %).
- Диссеминированное внутрисосудистое свертывание (ДВС): только в качестве крайней меры (Ultima Ratio), в большинстве своем без успеха.
- Спорно: при сепсисе или вирусной инфекции тяжелой степени.
Диагностические мероприятия перед каждым заменным переливанием
Мать: группа крови, непрямой тест Кумбса.
Ребенок: группа крови, прямой тест Кумбса, OAK с лейкоцитарной формулой, гематокритом и ретикулоцитами: билирубин. КОС и газовый состав: скрининг на болезни обмена веществ. При пороках развития (хромосомных заболеваниях) и прежде всего болезнях обмена веществ подумайте о заборе крови до проведения процедуры.
Если в основе заболевания не лежит обычная фетоматеринская несовместимость, ищите другие причины:
- Инфекционные. (TORCH, особенно ЦМВ), сепсис. Lues, листериоз.
- Гемолитическая анемия: ферментопатии (глюкозо-6-фосфат дегидрогеназа, пируваткиназа и т.д.), мембранопатии (врожденный сфероцитоз, эллиптоцитоз), гемоглобинопатии (α-талассемия: Hydrops); анемии, вызванные парвовирусом В 19 , ЦМВ.
- Галактоземии: скрининг на болезни обмена веществ.
- Несовместимость по редким группам крови (Kell, Anti-C).
- Кровоизлияния в кожу и полости тела (например, выраженная кефалогематома).
Практические рекомендации для заменного переливания крови новорожденному
Эритроцитарный концентрат (ЭК):
- При несовместимости по АВО-системе (0(1), Rh(-)) и АВ-плазма.
- При Rh-несовместимости группа крови как у ребенка, но Rh-отрицательная. Осторожно: антитела матери. Проведите предварительно пробу на совместимость ЭК и материнской крови (в отделении/станции переливания крови).
- Ощелачивание эритроцитарной массы: по Гашеку или вслепую на каждые 100 мл ЭК 0,8 мл TRIS 3 М.
- Облучение ЭК (10 мин). Осторожно: облученные эритроциты годны лишь ограниченное время.
- Подогрейте до температуры тела.
Количество: 2-3 ОЦК (ОЦК= 80 мл/кг) (при гипербилирубинемии); смешать с плазмой (как правило, 2:1), чтобы соответствовало гематокриту ребенка. Таким образом будет произведен обмен 90-95 % крови ребенка.
Доступ:
Забор крови можно осуществлять через пупочный артериальный катетер, трансфузию - через пупочный венозный катетер. Даже если катетеризация сосудов произведена только на короткий период, необходимо хорошо зафиксировать катетеры и по возможности выполнить рентген (осторожно, тромбоз портальной вены!).
Осторожно : забор крови из пупочной артерии осуществляйте маленькими порциями во избежание нарушения перфузии кишечника (иначе опасность развития НЭК).
Производите обменную трансфузию через периферический доступ (артерию и вену).
Преимущества:
- Возможен постоянный обмен без колебаний АД.
- Безопаснее с точки зрения развития тромбоза портальной вены.
Внимание , только в исключительных случаях производите забор из мелких артерий (например, a. radialis). В случае их использования набирайте кровь пассивным током, без активной аспирации (опасность нарушения перфузии). Перед каждой пункцией периферической артерии проверяйте перфузию конечности коллатеральными ветвями (тест Аллена).
Объем обмена : 2-3 мл/кг в одну порцию.
Внимание , заберите первые 10-20 мл крови ребенка (5-10 мл ЭДТА-кровь).
2 мл 10 % раствора кальция вводится после каждых 100 мл обмена (спорно).
Мониторинг : ЧСС, АД и ЧД (вести протокол). При колебаниях АД можно уменьшить запланированный объем обмена.
Лабораторный контроль : перед, во время и после обмена: электролиты (Na, К, Са), КОС и газовый состав, билирубин, общий белок, глюкоза крови и OAK (Ht, тромбоциты, лейкоциты).
Гипербилирубинемия .
- Производите заменное переливание крови медленно, минимум 2-3 часа, т.к. обмен между интра- и экстрацеллюлярным билирубином требует времени.
- Контроль билирубина каждые 3-6 часов (возможно, потребуется новая обменная трансфузия).
Обменная трансфузия при ДВС. наличии циркулирующих антител:
Обмен следует производить быстро - за один час.
Осторожно : опасность колебаний АД и развития отека легких.
Анемия около 1/3 объема следует заменять быстро (трансфузия, до Ht> 35 %), оставшийся объем медленно, за 2 часа.
Заменное переливание назначается новорожденным детям при тяжелых формах желтушных заболеваний. Данный способ лечения на сегодняшний день достаточно распространен, так как способствует наиболее быстрому решению проблемы. В первую очередь речь идет о выведении из организма токсических продуктов. Это может быть непрямой билирубин, большое количество эритроцитов, а так же множество других антител, который негативно влияют на здоровье новорожденных детей.
Нельзя с точностью сказать, что заболевание можно сразу вылечить одним только заменным переливанием крови. В данном случае все зависит от формы заболевания и ее прогрессировании.
Показания к переливанию
Переливание крови у детей должно проводиться только после назначений врача. Для этого есть соответствующие диагнозы, на которые и стоит ориентироваться. Например, одним из наиболее важных показателей является тот факт, что заметно ранее проявление болезни и ее быстрое нарастание. У детей это может быть ранняя желтуха, увеличение печени или селезенки, а так же появление большого количества молодых эритроцитов в крови.
Основным критерием для начала заменного переливания служит все же показатель билирубина. Если при рождении в пуповинной крови он становится больше 50 мкмоль/л, то это уже первый признак возможного дальнейшего переливания . Так же в этом случае нужно достаточно точно ориентироваться на скорость его накопления, так как в некоторых случаях терапию назначают в ускоренном виде. Опасным показателем скорости накопления непрямого билирубина является более 4,5 мкмоль/л в первые часы жизни новорожденного.
Как проводят заменное переливание
Данная процедура проводиться в объеме крови не больше 150-180 мл/кг. Это приблизительно 80% от общего количества всей циркулирующей крови новорожденного. Для этого используется исключительно подготовленная кровь, которая была выстояна не менее трех суток – это свежая кровь. Все показатели донорства в данном случае так же важны, как и при других процедурах. Поэтому, в любом случае должен быть подобран донор.
Даже если мать подходит в качестве донора, то ее кровь не допускается брать в течение двух месяцев после родов. Это в первую очередь говорит о том, что организм матери должен и так восстановиться после кровопотерь и быть крепким для дальнейшей лактации.
При переливании возможна замена только эритроцитов отдельно от плазмы. В данном случае используется пупочная вена новорожденного при соблюдении всех правил переливания. Предварительно нужно через катетер вывести 10-15 мл крови от ребенка, а после вводить замену в нужном количестве. Так же в этой процедуре переливания очень важно следить за скоростью, ведь она не должна превышать больше 2-3 мл/минуту.
Как правило, общая продолжительность переливания крови занимает около двух часов. В течение этого времени через каждый 100 мл дополнительно в вену вводят раствор кальция хлорида. Такое заменное переливание у детей позволяет вовремя предупредить смерть или распространение дальнейшего заболевания. Как следствие этого, из организма ребенка выводиться непрямой билирубин и наступает постепенное выздоровление. Именно большое количество токсичного непрямого билирубина может быть смертельной дозой для новорожденных детей.
Из-за чего приходиться делать переливание
 Первой причиной заменного переливания, как было указано ранее, является повышенное количество непрямого билирубина. Из-за этого у детей наблюдается желтая окраска тела. Это свидетельствует об разрушении красных кровянистых клеток. Большое количество билирубина существенно и быстро распространяется по крови новорожденного и постепенно поражает печень, кишечник, а кожа соответственно приобретает желтоватый цвет. Таким образом, уже в течение двух часов после рождения детей можно определить первые симптомы повышенного содержания билирубина. Важно учитывать, что при переливании могут возникнуть .
Первой причиной заменного переливания, как было указано ранее, является повышенное количество непрямого билирубина. Из-за этого у детей наблюдается желтая окраска тела. Это свидетельствует об разрушении красных кровянистых клеток. Большое количество билирубина существенно и быстро распространяется по крови новорожденного и постепенно поражает печень, кишечник, а кожа соответственно приобретает желтоватый цвет. Таким образом, уже в течение двух часов после рождения детей можно определить первые симптомы повышенного содержания билирубина. Важно учитывать, что при переливании могут возникнуть .
Вероятность возникновения физиологической желтухи у новорожденных
К сожалению, почти у 60% доношенных детей на 3-4 день проявляется физиологическая желтуха. На сегодняшний день причин этому еще не выявлено, но с уверенностью можно перечислить основные показатели, характеризующие это заболевание:
- у новорожденных детей наблюдается разрушение эритроцитов, что обусловлено заменой плодного гемоглобина;
- в качестве следующего симптома для переливания могут послужить некоторые осложнения при родах, что дали толчок для сильного выброса непрямого билирубина;
- идет осложнение работы печени, так как это единственный орган, который в данный момент будет отвечать за выведение его из организма;
- так как печень малыша не созрела до сих пор для такой активной работы, то она может постепенно снижать свою продуктивность, что в свою очередь будет затруднять работу организма таких маленьких детей.
Всегда ли виновата только печень в повышении уровня билирубина:
